がん治療がん遺伝子治療
本来ヒトが持っているがん抑制遺伝子を復活させることで
がんを抑制する治療
がんと遺伝子
私たちの細胞は、細胞分裂して増加し、そして新しい細胞に置き換わるという作業を繰り返しています。この際、自己の細胞は中に入っている様々な物質をコピーしながら増えていきますが、一番大事な情報の詰まった遺伝子自身もコピーを行います。ここに化学物質や紫外線など、遺伝子を傷つける刺激があった場合には、傷があるままコピーすると困るので、修復する機能の遺伝子も持っています。ところがこの修復遺伝子が壊れるとどうなるでしょうか?遺伝子の故障を治せないばかりかおかしな細胞をコピーしてしまうことになります。また、本来これくらいの回数コピーしたら寿命を迎えましょうという働き(いわゆる自殺する)の遺伝子も壊れてしまった場合は、無限に増殖する異常なコピー細胞が増え続けることになります。これがいわゆる、がん細胞です。
上記の内容の修復や自殺をする遺伝子をがん抑制遺伝子と呼びますが、この本来の正常細胞が持っていたはずのがん抑制遺伝子をがん細胞の中に発現させ自殺に導くのが、がん遺伝子治療です。
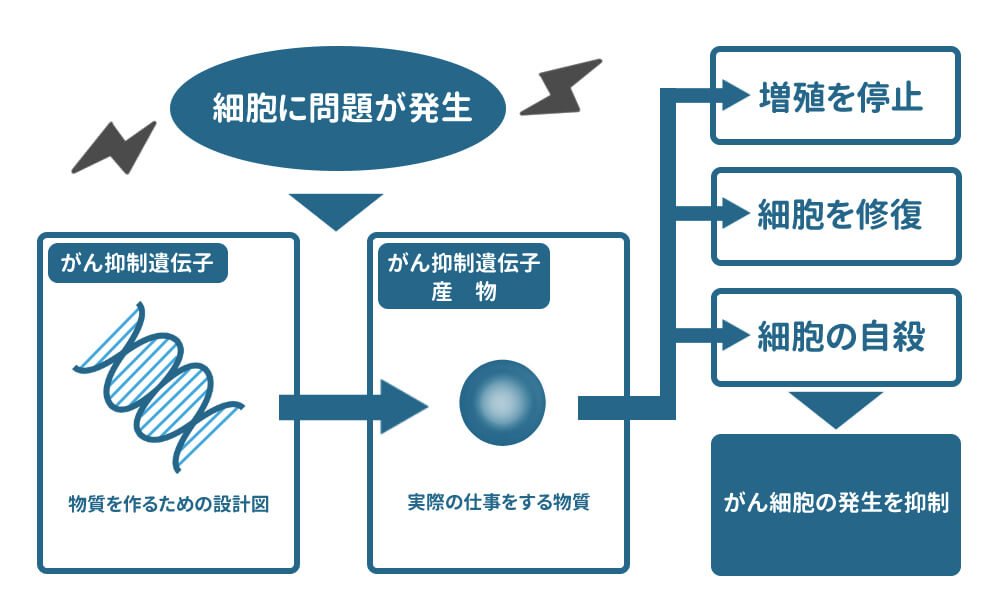
がん抑制遺伝子は、がんの発生を未然に防ぐ働きを持った物質(がん抑制遺伝子産物)を作り出し、細胞のがん化にストップをかけます。抑制の方法は以下の3種類です。
(1)細胞の増殖を停止する
(2)壊れた細胞の機能を修復する
(3)細胞を自殺させる(アポトーシス)

がん細胞はがん抑制遺伝子が壊れてしまっているので以下のことが起こります。
(1)自律性増殖:自律的に無限に増殖を続ける。
(2)浸潤と転移:周囲に染み出るように広がり(浸潤)、あちこちに転移する。
(3)悪液質:他の正常組織の栄養を奪って体を衰弱させる。

当院のがん遺伝子治療
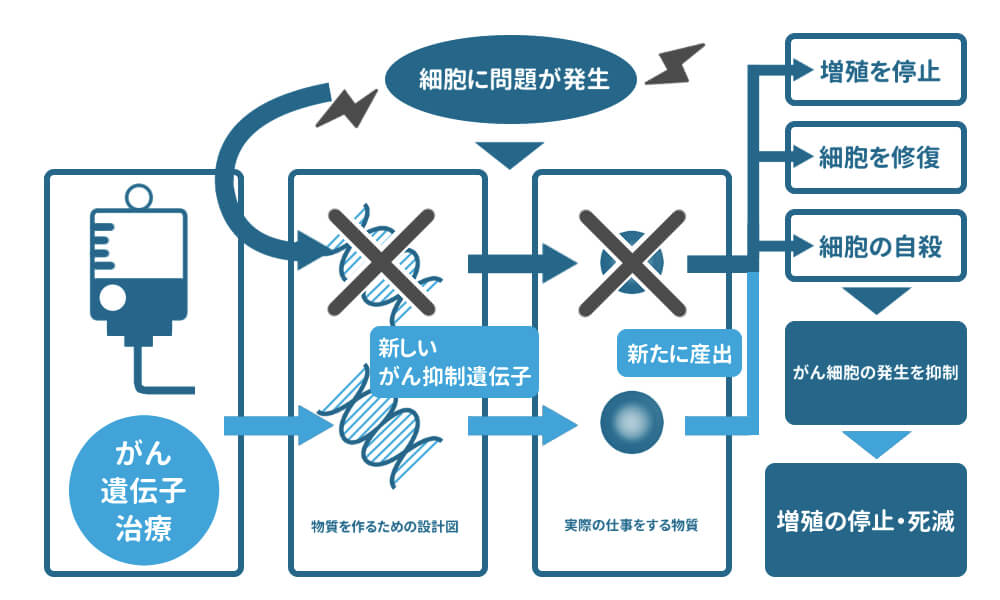
遺伝子をがん細胞に運ぶ仕組み
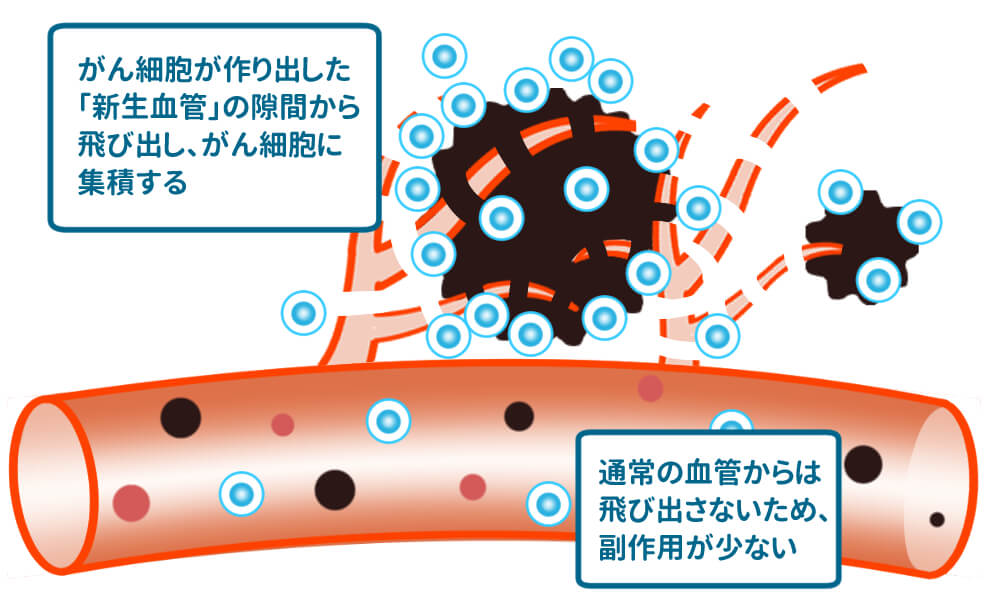
EPR効果
がん細胞は盛んに分裂や増殖を行うために、周囲の毛細血管から新しい血管(新生血管)を作りだし、酸素や栄養をそこから取り込もうとします。新生血管は血管壁が正常血管よりも粗く、100〜200nm(ナノメートル)程度の隙間が空いています。抗がん剤やがん治療に使う遺伝子、そして光感作物質の大きさは、通常で1nm(ナノメートル)以下の低分子です。この大きさのまま体内に投与すると、正常血管からも漏れ出してしまい、がんになっていない正常な組織にも届いて細胞を破壊してしまいます。抗がん剤などで副作用が出るのはこのためです。
そこで、正常血管からは漏れ出さずに、がん細胞が作り出す新生血管からだけ漏れ出すように、薬剤等の大きさを100nm(ナノメートル)程度に加工します。これらは、正常血管からは漏れ出さず、新生血管からのみ漏れ出すので、がん細胞に集中的に蓄積されます。さらに、漏れ出した薬剤等は再び血管内に戻りにくく、がん細胞周辺に留まります。EPR効果はノーベル賞候補にもなった熊本大学名誉教授の故・前田浩氏が発見しました。
がん遺伝子治療の特徴
がん遺伝子治療は、がん抑制遺伝子を投与して、本来の体内に備わっているがん抑制機構を再び機能させるための治療です。人間の身体に備わった機能に根ざした治療であるため、苦痛や副作用などの負担が少ない、身体に優しい治療です。
がん抑制機構が回復することにより、抗がん剤治療や放射線治療など他の治療との併用により効果が高まる可能性があります。当院でも標準治療との併用でも多くの著効を上げています。がん遺伝子治療は他の治療のスケジュールに合わせながら、また通常の生活を送りながらの通院治療も可能です。
点滴によりがん細胞にのみ集積しアポトーシスに誘導する治療ですので、遠隔転移がある進行性のがん(末期がん、ステージⅣ)などでも適応が可能です。
がん遺伝子治療に用いる遺伝子
遺伝子の司令塔
p53
細胞の危険信号を察知すると活性化するがん抑制遺伝子です。がんを防ぐために、さまざまな遺伝子に命令を出すため「ゲノムの守護者」と呼ばれています。DNAの傷の修復・過剰な細胞増殖を抑制・損傷細胞のアポトーシス(自死)を行い、がん細胞を消し去ります。このp53はあらゆるがんに発現していることが分かっており、おおよそほとんどのがんへの遺伝子治療に使用する重要な遺伝子です。またがん細胞の中には、このp53を有効に働かせないようにするタンパク質を作る遺伝子を持っているものもいますので、ただp53を入れるだけでは改善できない場合があります。そこで当院の遺伝子治療では、p53の投与の前準備としてp53を阻害するたんぱくを抑制する遺伝子を投与することで、p53本来の働きを十二分に発揮するようにプログラムしております。
がん細胞を選択的に攻撃
TRAIL
TNF(Tumor Necrosis Factor・腫瘍壊死因子)ファミリーに属する免疫システムのサイトカイン伝達物質です。正常組織には影響を与えずに、がん細胞の表面にのみ結合してアポトーシス誘導シグナルを伝達します。TRAILの働きはNK(ナチュラルキラー)細胞療法をはじめとする、免疫療法を強化する作用もありますので、組み合わせて行うこともあります。
がん細胞に初期対応
p16
p16は細胞周期の調整に重要な役割を果たしているタンパク質です。細胞周期を停止させて、老化させることで異常な細胞増殖を防ぎます。正常な細胞ではp16はほとんど機能しません。p16は肺がん、膵臓がん、腎臓がん、子宮がん、乳がんなどで壊れている場合が多く、なかでもホルモン療法が効果のある乳がん(エストロゲンレセプター反応性)の方の、ホルモン療法の成功率を妨げる因子としてp16の異常が多くみられるとする報告もあります。当院の遺伝子治療ではp53や他の遺伝子とともに投与を行います。
がん細胞増殖を抑制
CDC6
CDC6は、細胞を増殖させるために働くタンパク質で、細胞周期調整因子のひとつです。がん細胞にはこのCDC6が過剰に発現することから、これを阻害するCDC6shRNAを投与することで、がん細胞の増殖停止やアポトーシスに導きます。
がん原遺伝子を制御
PTEN
アポトーシスの抑制や、細胞増殖に関与しているがん原遺伝子「AKT」の働きを制御する酵素です。PTENが異変や欠損している細胞では癌化が発生し、単球浸潤などの炎症や腫瘍血管新生の誘導などが起こり、がんの増殖が加速するので、正常なPTENを投与することで、がんの増殖に歯止めをかける治療になります。PTENの異常は前立腺がん、膵臓がん、乳がん、子宮がん、大腸がんなどで異常を起こしている場合が多く報告されています。
がん細胞分裂を制御
Rb
網膜芽細胞腫(Retinoblastoma)の原因遺伝子として初めて発見されたもので、細胞分裂が進むのを抑制する働きがあります。この異常があるがんでは、細胞がどんどん分裂し増殖していきます。網膜芽細胞腫以外でも、肺の小細胞がん、骨肉腫などで多く異常が報告されています。
様々ながん形成に関係
CDK4
この遺伝子の変異は、p16やRb遺伝子などと関わり、様々な種類のがんにおいて腫瘍形成に関係しています。p16やRb遺伝子治療の前に投与していくことが多く、組み合わせて使用します。またリボシクリブはCDK4とCDK6の阻害剤として、エストロゲン受容体陽性/HER2陰性の進行性乳がんに対する治療薬としてアメリカ食品医薬品局(FDA)に承認されています。また軟部肉腫など希少癌でも多く異常がみられることから幅広い癌に関係しているとみられます。
p53とRbとの併用で効果
PSMD10(ガンキリン)
がん抑制に重要な働きをするp53、Rb、PTEN遺伝子を十分に働かせるために使用します。過去の報告では単独での治療効果はあまりあがらないようですが、p53やRbと組み合わせることで効果が期待できます。
細胞分裂を促進しp53を阻害
MDM2
代表的なp53を阻害するものがMDM2タンパク質です。MDM2は細胞分裂促進機能があるため、正常細胞では組織の修復にも関与しています。しかし、p53が壊れた状態のがん細胞は、細胞の増殖を促進しているので、MDM2タンパク質をコードする遺伝子にブレーキをかけることで正常なp53を働きやすくします。
細胞増殖のアクセル役
KRAS
EGFR(上皮成長因子受容体)からの細胞増殖のシグナルを核に伝達し、細胞増殖を進めるアクセルとしての機能を持っています。分子標的薬といわれるアービタックスやベクティビックスはEGFRをターゲットにした治療薬ではありますが、このKRAS遺伝子に変異がある大腸がんの患者さまには効果がないという事が報告されており、実際に治療前にはKRAS遺伝子の変異があるかどうかを検査で判定し、分子標的薬の使用を検討します。実際日本人の大腸がんの40%程度はKRAS変異があるため、半分弱の大腸がんの患者さまは、これら分子標的薬が効かないという事になります。遺伝子治療ではKRASのがん細胞を増殖させる働きを抑制させることを狙います。特に膵臓がんや肺腺がん、大腸がんに異常を認めることが多いです。
どの遺伝子を選択するかは、2つの方法があります
- 血液より末梢循環腫瘍細胞(CTC)の遺伝子異常を同定してから、それに合わせて治療を計画する方法です。 確信をもって遺伝子材料を選択できますが、結果が出るのにおよそ1か月程度要するため、その期間は他の治療でがんの進行を遅らせながら結果を待ちます。
- 原発部位から報告されている遺伝子異常をもとに、数種類を組み合わせてプログラムする方法です。 一見乱暴な選択の仕方にも思えるかもしれませんが、遺伝子研究は日進月歩であり、世界中の論文などで、各がんの原因遺伝子異常が報告されているため、当院では絶えず情報をアップデートしながら遺伝子の組み合わせを進化させています。この方法でプログラムした場合と、①の方法で選択した場合は、治療遺伝子の種類はほとんど一致していますので、治療を開始する待ち時間を短縮できかつ正確性もあるといえます。やはり遺伝子治療も、少しでも早く開始したほうが効果は上がりやすい傾向があります。
遺伝子治療との併用療法
遺伝子が正常に働きやすく、また、がん細胞の自殺をより誘導しやすくするため、サプリメントなどの内服治療を平行でお勧めしています。がん種によってはサプリメントをメインに遺伝子治療を補助的にお勧めする場合もあります。例えば、当院で行っておりますヨウ素療法は、がん抑制遺伝子のp53を誘導し、PTENを活性化しますので、遺伝子治療と合わせてプログラムしています。
がん遺伝子治療の適応について
一部の特殊ながん・小児がんを除いて治療対象になります。また一回の治療は点滴で40分程度ですので、食事がとれない方や歩行するのも体力的に厳しい方でも治療可能です。詳しくはお問い合わせください。
大腸がん、直腸がん、十二指腸がん 膵臓がん 食道がん 胃がん 肝がん 腎がん 胆管がん 膀胱がん 前立腺がん 甲状腺がん メラノーマ 肺がん 乳がん 子宮体がん 子宮頸がん 卵巣がん 口腔がん 喉頭がん 咽頭がん など
※詳しくは医師にお問い合わせください。
こんな方が受けられています
- 副作用が少ないがん治療をご希望の患者さま
- 抗がん剤や放射線治療との併用を考えられている患者さま
- 抗がん剤などが使用できないなど、保険治療での加療方法がない患者さま
リスク・副作用
体細胞に特定の遺伝子断片を導入することによってがん細胞の発生抑制を図る治療です。遺伝子投与による次世代への影響はございません。
- 点滴の際に、まれに皮下血腫・神経損傷などの合併症が起きることがあります。
- 初回の点滴後に微熱がみられることがあります。(1%程度)
- すべての方に効果が現れるものではありません。
当院ではこれまでに重篤な副作用は見受けられていません。しかし、世界中で遺伝子治療が行われており、様々な副作用が報告されています。使用している遺伝子材料がクリニックによって違いますので、当院では国内の信頼できる研究所との提携で安心できる材料を使用しております。下記に他施設で報告されているものを列記します。
蕁麻疹、吐き気、軽度の白血球減少、腎機能障害、血液凝固障害など
報告だけみると、不安になられるかと思いますが、実際にどこの国のどの研究機関と材料提携するかが安全面において非常に重要だと思います。
当院で採用しています(2021年現在)遺伝子材料での副作用は、微熱が初回点滴をした日の夜間に見られる程度で、どの方も2回目以降には発熱はありません。
ただし、以下の患者さまについては、治療対象から除外されます
1) 重篤なアレルギーを有する、あるいは既往のある患者さま
2) 子ども、妊娠中の女性、妊娠が疑われる女性、あるいは授乳中の患者さま
3) その他、本治療により不利益を受けると予測される患者さま、および本人ならびに家族(あるいは親族)の文書による同意が得られない患者さまなど
治療の流れ
STEP-1 初診医師が、治療の内容について詳しくご説明いたします。
STEP-2 治療計画立案患者さまごとに計画します。
STEP-3 遺伝子投与1回40分程度の外来点滴 6回を1クールで行います。
遺伝子期間中、サプリメントなどの内服を併用することもあります。
STEP-4 効果判定画像や血液データ(腫瘍マーカー)、CTC検査の結果を参考にその後継続可能な治療のプログラミングを行います。
承認医薬品等であることの明示、入手経路等の明示
本治療に用いる遺伝子は、医療機器等法上の承認を得ていないものです。院内調剤(一部外部 委託)として、適法に調剤しています。 日本では、未承認医薬品を医師の責任において使用することができます。
国内の承認医薬品等の有無の明示
本治療に使用できる同一の性能を有する他の国内承認医薬品はありません。
諸外国における安全性等に係る情報の明示
Germline-integrationのリスク評価
General Principles to Address the Risk of Inadvertent Germline Integration of Gene Therapy Vectors Oct. 2006
